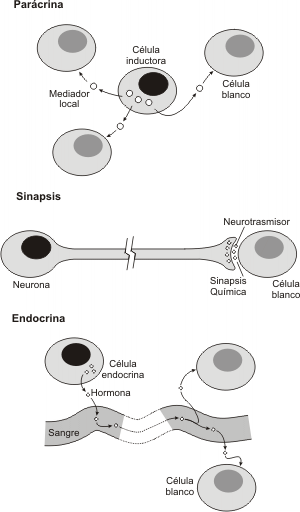
Modelos de comunicación celular
Bases Molecular de la comunicación Intercelular
Los organismos unicelulares pueden realizar todas las funciones necesarias para mantener la vida. Por ejemplo, una ameba, organismo unicelular, asimila los nutrientes del medio, se mueve, lleva a cabo las reacciones metabólicas de síntesis y degradación y se reproduce. En los organismos pluricelulares, la situación es mucho más compleja, ya que las diversas funciones celulares se distribuyen entre distintas poblaciones de células , tejidos y órganos. De este modo en un organismo pluricelular, cada célula depende de otras y las influye. Por lo tanto la mayoría de las actividades celulares, solo se desarrollan, si las células involucradas son alcanzadas por estímulos provenientes de otras. Para coordinar todas estas diversas funciones deben existir mecanismos de comunicación intercelular.
Cuando una célula recibe un estímulo puede responder con alguno de los siguientes cambios, dependiendo de las características del estímulo y el tipo de célula receptora del mismo: por ejemplo, se puede diferenciar, reproducir, incorporar o degradar nutrientes, sintetizar, secretar o almacenar distintas sustancias, contraerse, propagar señales o morir.
Inducción
En la mayoría de los organismos superiores existen dos métodos fundamentales de comunicación intercelular: un sistema fundado en las neuronas o células nerviosas y otro basado en las hormonas. En ambos sistemas las células se comunican entre si a través de mensajeros químicos.
Las neuronas envían mensajes a sus células efectoras (células blanco), que pueden ser células musculares, células glandulares u otras neuronas. Para enviar su mensaje, la neurona libera una sustancia química, un neurotransmisor. El neurotransmisor es liberado en sitios específicos llamados sinapsis. Las moléculas de neurotransmisor se unen a receptores, situados en la superficie de la célula blanco, y provocan de esta forma cambios físicos y químicos en la membrana celular y en el interior celular.
Por lo tanto diremos que en general, la acción de estimular a las células desde el exterior se llama inducción y se realiza a través de sustancias producidas por células inductoras. La célula que es sensible al inductor se denomina célula inducida, blanco o diana y presenta para el mismo receptores específicos, que pueden ubicarse en la membrana plasmática, el citoplasma o en el núcleo. Estos receptores son proteínas o complejos proteicos.
Cuando el receptor se encuentra en el citoplasma o en el núcleo, el inductor debe ser pequeño e hidrófobo, de modo que pueda atravesar la membrana plasmática sin dificultad, mientras que los receptores de membrana pueden recibir inductores de cualquier tipo.
La acción de las hormonas, puede darse básicamente de acuerdo a uno de estos cinco tipos de inducción:
1. Endocrina: una glándula libera hormonas (inductor) que pueden actuar sobre células u órganos situados en cualquier lugar del cuerpo (células blanco). Por lo tanto podemos decir que células inductoras e inducidas se encuentran distantes. Las glándulas endocrinas liberan hormonas al torrente sanguíneo: las células o tejidos blanco poseen receptores que reconocen exclusivamente los diferentes tipos de moléculas hormonales. Así un receptor reconoce exclusivamente una hormona. Una célula puede tener distintos tipos de receptores, y así reconocer diferentes hormonas. Ej. Insulina, glucagón, hormonas adenohipofisiarias, etc.
2. Paracrina: Una célula o un grupo de ellas liberan una hormona que actúa sobre las células adyacente que presenten el receptor adecuado. De esta forma la célula inductora e inducida se encuentran próximas. Ej. Prostaglandinas
3. Autocrina: Una célula libera una hormona que actúa sobre la misma célula. Ej. prostaglandinas
4. Neuroendocrina: Una neurona libera su neurosecreción al torrente sanguíneo. Ej. Oxitocina, ADH, hormonas liberadoras e inhibidoras hipotalámicas
5. Por contacto directo: La hormona o molécula inductora es retenida en la membrana plasmática de la célula inductora, por lo tanto no se secreta. Las células deben ponerse en contacto, para que la sustancia inductora tome contacto con el receptor localizado en la membrana plasmática de la célula inducida. Ejemplo de este tipo de comunicación tienen lugar en algunas respuestas inmunológicas.
6. Yuxtacrina: ( a través de uniones comunicantes, nexus o gap: Las células conectadas a través del establecimiento de este tipo de uniones firmes, puede responder de forma coordinada ante un inductor que se une a alguna de las células que están comunicadas. A través de estas uniones pasan pequeñas moléculas como los segundos mensajeros.
BIBLIOGRAFÍA
- MARQUÉS, Silvia. GENOMA SUR, comunicación intercelular y transmisión de señales. [en línea]
<http://genomasur.com/lecturas/Guia07.htm>
[citado el día 2 de Noviembre del 2010]